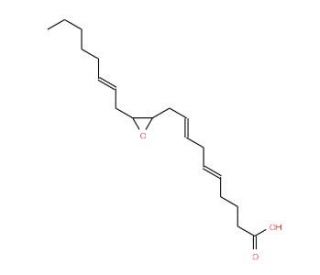

(±)11(12)-EET (CAS 81276-02-0)
Direktverknüpfungen
(±)11(12)-EET ist eine Verbindung, die bei zellulären Prozessen als Signalmolekül fungiert. Sie wirkt als Epoxygenase-Metabolit von Arachidonsäure und spielt eine Rolle bei der Regulierung des Gefäßtonus und der Entzündung. Auf molekularer Ebene interagiert (±)11(12)-EET mit spezifischen Rezeptoren, um intrazelluläre Signalwege zu modulieren und die Expression von Genen zu beeinflussen, die an der Regulierung von Blutdruck und Entzündungen beteiligt sind. (±)11(12)-Eet ist an der Modulation von Ionenkanälen und Enzymen beteiligt und trägt so zur Regulierung des Tonus der glatten Gefäßmuskulatur und der Funktion der Endothelzellen bei. (±)11(12)-EET kann Auswirkungen auf das kardiovaskuläre System haben, einschließlich der Regulierung des Blutflusses und der Modulation von Entzündungsreaktionen. Sein Wirkmechanismus beinhaltet die Aktivierung spezifischer zellulärer Signalwege, die letztlich physiologische Prozesse im Zusammenhang mit der Gefäßfunktion und Entzündungen beeinflussen.
(±)11(12)-EET (CAS 81276-02-0) Literaturhinweise
- Cytochrom P450 und die Bioaktivierung von Arachidonsäure. Molekulare und funktionelle Eigenschaften der Arachidonat-Monooxygenase. | Capdevila, JH., et al. 2000. J Lipid Res. 41: 163-81. PMID: 10681399
- 11,12-Epoxyeicosatriensäure (11,12-EET): strukturelle Determinanten für die Hemmung der TNF-alpha-induzierten VCAM-1-Expression. | Falck, JR., et al. 2003. Bioorg Med Chem Lett. 13: 4011-4. PMID: 14592496
- Arachidonsäure hemmt basolaterale K-Kanäle in den kortikalen Sammelkanälen über Cytochrom P-450 Epoxygenase-abhängige Stoffwechselwege. | Wang, Z., et al. 2008. Am J Physiol Renal Physiol. 294: F1441-7. PMID: 18417544
- Arachidonsäure-Cytochrom-P450-Epoxygenase-Weg. | Spector, AA. 2009. J Lipid Res. 50 Suppl: S52-6. PMID: 18952572
- Eine hohe Kaliumzufuhr verstärkt die hemmende Wirkung von 11,12-EET auf ENaC. | Sun, P., et al. 2010. J Am Soc Nephrol. 21: 1667-77. PMID: 20595684
- 11,12-Epoxyeicosatriensäure induziert eine gefäßerweiternde Reaktion in den durchbluteten Mesenterialgefäßen der Ratte. | Bihzad, SM. and Yousif, MH. 2017. Auton Autacoid Pharmacol. 37: 3-12. PMID: 28332266
- 11,12 -Epoxyeicosatriensäure (11,12 EET) reduziert die Erregbarkeit und die Erregungsübertragung im Hippocampus. | Mule, NK., et al. 2017. Neuropharmacology. 123: 310-321. PMID: 28526610
- Lipidmetaboliten der Cytochrom-P450-Monooxygenase sind wichtige Botenstoffe bei der Auflösung von choroidalen Neovaskularisationen. | Hasegawa, E., et al. 2017. Proc Natl Acad Sci U S A. 114: E7545-E7553. PMID: 28827330
- Zeitaufgelöste phosphoproteomische Analyse klärt hepatische 11,12-Epoxyeicosatriensäure-Signalwege auf. | Rahm, M., et al. 2020. Prostaglandins Other Lipid Mediat. 146: 106387. PMID: 31669255
- Die neovaskulogene Wirkung von 11,12-Epoxyeicosatriensäure betrifft die Akt/eNOS-Signalwege in menschlichen endothelialen Vorläuferzellen. | Hung, HC., et al. 2022. Biomedicine (Taipei). 12: 20-30. PMID: 36381190
- Oxygenierung von Arachidonsäure durch hepatische Monooxygenasen. Isolierung und Metabolismus von vier Epoxid-Zwischenprodukten. | Oliw, EH., et al. 1982. J Biol Chem. 257: 3771-81. PMID: 6801052
- Neue Epoxide, die bei der Cytochrom P-450-Oxidation von Arachidonsäure in der Leber entstehen. | Chacos, N., et al. 1982. Biochem Biophys Res Commun. 104: 916-22. PMID: 6803794
- Die Wiederherstellung der Ca2+-Pools und des Wachstums in Zellen, denen der Ca2+-Pool fehlt, wird durch spezifische Epoxyeicosatriensäuren vermittelt, die von Arachidonsäure abgeleitet sind. | Graber, MN., et al. 1997. J Biol Chem. 272: 29546-53. PMID: 9368016
Bestellinformation
| Produkt | Katalog # | EINHEIT | Preis | ANZAHL | Favoriten | |
(±)11(12)-EET, 25 µg | sc-220579 | 25 µg | CNY553.00 | |||
(±)11(12)-EET, 50 µg | sc-220579A | 50 µg | CNY1004.00 |
