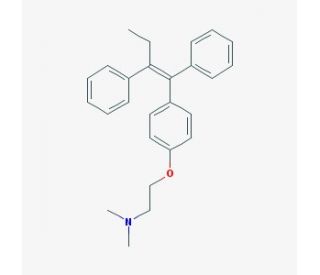
Tamoxifen (CAS 10540-29-1)
Voir les citations produits (18)
ACCÈS RAPIDE AUX LIENS
Le tamoxifène est un modificateur sélectif de la réponse aux œstrogènes (SERM), qui offre un mécanisme nuancé de modulation de l'activité des récepteurs d'œstrogènes. Son rôle s'étend à l'inhibition de la protéine kinase C (PKC), une enzyme centrale dans les voies de signalisation cellulaire qui influencent la croissance et la différenciation des cellules, mettant en évidence son potentiel dans la recherche axée sur la régulation cellulaire et la transduction des signaux. En outre, le tamoxifène présente des propriétés anti-angiogéniques, empêchant le développement de nouveaux vaisseaux sanguins, ce qui est crucial dans l'étude de la croissance des tumeurs et des métastases. Le tamoxifène est transformé par les isoformes CYP2D6 et CYP3A4 du cytochrome P450 en ses métabolites actifs, le 4-hydroxytamoxifène (4-OHT) et l'endoxifène, qui sont au cœur de son mécanisme d'action. Cette transformation souligne l'importance des voies métaboliques dans la modulation de l'activité des composés. Dans le contexte de la recherche sur le cancer du sein, la capacité du tamoxifène à agir comme un répresseur de gènes contre ERBB2 par le biais de la dépendance à PAX2 met en évidence son potentiel dans les études d'expression génique et l'exploration des mécanismes de régulation génétique. Son efficacité à bloquer la production de VEGF stimulée par l'œstradiol dans les cellules tumorales du sein souligne encore son rôle dans la dissection des processus hormonaux de l'oncogenèse. En outre, l'induction de l'apoptose par le tamoxifène dans les lignées cellulaires de gliomes malins humains constitue un modèle pour l'étude des mécanismes de mort cellulaire programmée. En tant qu'activateur des récepteurs d'œstrogènes alpha (ER alpha) et bêta (ER bêta), le tamoxifène facilite l'exploration des voies de signalisation des récepteurs d'œstrogènes, contribuant ainsi de manière significative à une meilleure compréhension des réponses cellulaires à la stimulation hormonale.
Tamoxifen (CAS 10540-29-1) Références
- Étude par modélisation moléculaire des interactions entre le tamoxifène, un médicament anti-œstrogène, et plusieurs de ses dérivés, et la calmoduline, une protéine liant le calcium. | Edwards, KJ., et al. 1992. J Med Chem. 35: 2753-61. PMID: 1322985
- TGFbeta2 et TbetaRII sont des biomarqueurs moléculaires valables pour les effets antiprolifératifs du tamoxifène et de ses métabolites sur les cellules du cancer du sein. | Buck, MB., et al. 2008. Breast Cancer Res Treat. 107: 15-24. PMID: 18043895
- Amino et iodotamoxifènes: synthèse, affinité pour les récepteurs d'œstrogènes et biodistribution. | Strickland, LA., et al. 1990. Drug Des Deliv. 6: 195-212. PMID: 1963782
- Séparation des isomères du métabolite du tamoxifène et quantification par chromatographie liquide et spectrométrie de masse en tandem. | Jaremko, M., et al. 2010. Anal Chem. 82: 10186-93. PMID: 21086978
- Arylation oxydative de Heck pour la synthèse stéréosélective d'oléfines tétrasubstituées en utilisant des nitroxydes comme oxydants. | He, Z., et al. 2012. Angew Chem Int Ed Engl. 51: 3699-702. PMID: 22383123
- Effets opposés du tamoxifène sur l'activité de la protéine kinase C in vitro et sur la phosphorylation des protéines endogènes dans les cellules MCF-7 intactes. | Issandou, M., et al. 1990. Cancer Res. 50: 5845-50. PMID: 2393853
- Synthèse stéréosélective de triaryléthylènes par couplage décarboxylatif catalysé par le cuivre et le palladium: synthèse du (Z)-tamoxifène. | Cahiez, G., et al. 2014. Chem Commun (Camb). 50: 8982-4. PMID: 24980393
- Synthèse et évaluation biologique de nouveaux conjugués tamoxifène-1,2,4-triazole. | Murty, MS., et al. 2016. Mol Divers. 20: 687-703. PMID: 27278444
- Les isomères et les métabolites du tamoxifène présentent une affinité et une activité distinctes pour les récepteurs cannabinoïdes: Un échafaudage potentiel pour le développement de médicaments. | Ford, BM., et al. 2016. PLoS One. 11: e0167240. PMID: 27936172
- Le tamoxifène, un médicament pionnier: Une mise à jour du potentiel thérapeutique des dérivés du tamoxifène. | Shagufta,. and Ahmad, I. 2018. Eur J Med Chem. 143: 515-531. PMID: 29207335
- Inhibition de la protéine kinase C par le tamoxifène. | O'Brian, CA., et al. 1985. Cancer Res. 45: 2462-5. PMID: 3157445
- Aspects du métabolisme du tamoxifène par les microsomes hépatiques de rat. Identification d'un nouveau métabolite: E-1-[4-(2-dimethylaminoethoxy)-phenyl]-1, 2-diphenyl-1-buten-3-ol N-oxide. | McCague, R. and Seago, A. 1986. Biochem Pharmacol. 35: 827-34. PMID: 3954788
- Pharmacologie du tamoxifène chez les animaux de laboratoire. | Jordan, VC., et al. 1980. Cancer Treat Rep. 64: 745-59. PMID: 6775807
- Détermination des produits pharmaceutiques et des impuretés connexes par électrophorèse capillaire. | Ng, CL., et al. 1994. J Chromatogr A. 680: 579-86. PMID: 7981835
- L'action antioxydante d'un antioestrogène pur: capacité à inhiber la peroxydation des lipides par rapport au tamoxifène et au 17 bêta-oestradiol et pertinence pour son potentiel anticancéreux. | Wiseman, H. 1994. Biochem Pharmacol. 47: 493-8. PMID: 8117317
Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
Tamoxifen, 2.5 g | sc-208414 | 2.5 g | CNY3069.00 |
