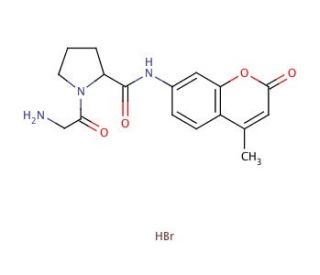
Structure moléculaire de GP-AMC, Fluorogenic Substrate, Numéro CAS: 115035-46-6
GP-AMC, Fluorogenic Substrate (CAS 115035-46-6)
Noms alternatifs:
Gly-Pro-7-amido-4-methylcoumarin hydrobromide; Gly-Pro-AMC
Application(s):
GP-AMC, Fluorogenic Substrate est utilisé pour étudier l'activité de CD26, DPP7, DPP8, FAP et PREP
Numéro CAS:
115035-46-6
Pureté:
>97%
Masse Moléculaire:
410.3
Formule Moléculaire:
C17H19N3O4•HBr
Pour la Recherche Uniquement. Non conforme pour le Diagnostic ou pour une Utilisation Thérapeutique.
* Consulter le Certificat d'Analyses pour les données spécifiques à un lot (incluant la teneur en eau).
ACCÈS RAPIDE AUX LIENS
Informations pour la commande
Description
Information Technique
Données de Sécurité
SDS & Certificat d’Analyses
GP-AMC, substrat fluorogène est un substrat avec une excitation à 380 nm et une émission à 460 nm. Le substrat a été utilisé pour étudier l'activité de CD26 (DPIV et DPPIV), DPP7 (DPPII/VII), DPRP1 (DPP8), DPRP2 (DPP9), FAP (protéine d'activation des fibroblastes) et POP/PREP. Le composé a été utilisé dans un essai peptidique où la libération de l'AMC a été surveillée, ainsi que dans un criblage d'inhibiteurs in vitro.
GP-AMC, Fluorogenic Substrate (CAS 115035-46-6) Références
- Les peptides antigéniques présentés par le complexe majeur d'histocompatibilité de classe I sont dégradés dans les extraits cytosoliques principalement par la thimet oligopeptidase. | Saric, T., et al. 2001. J Biol Chem. 276: 36474-81. PMID: 11479311
- Spécificité du substrat, inhibition et analyse enzymologique de la glutamate carboxypeptidase II humaine recombinante. | Barinka, C., et al. 2002. J Neurochem. 80: 477-87. PMID: 11905994
- Propriétés catalytiques et inhibition des dipeptidyl peptidases II, IV et VII spécifiques de la proline. | Leiting, B., et al. 2003. Biochem J. 371: 525-32. PMID: 12529175
- 1-[[(3-hydroxy-1-adamantyl)amino]acétyl]-2-cyano-(S)-pyrrolidine: un inhibiteur de la dipeptidyl peptidase IV puissant, sélectif et biodisponible par voie orale, doté de propriétés antihyperglycémiques. | Villhauer, EB., et al. 2003. J Med Chem. 46: 2774-89. PMID: 12801240
- Caractérisation de la dipeptidyl peptidase IV humaine exprimée dans Pichia pastoris. Comparaison structurelle et mécanistique entre l'enzyme humaine recombinante et l'enzyme porcine purifiée. | Bär, J., et al. 2003. Biol Chem. 384: 1553-63. PMID: 14719797
- Synthèse diastéréosélective et activité dépendant de la configuration de (3-substitués-cycloalkyl)glycine pyrrolidides et thiazolidides en tant qu'inhibiteurs de la dipeptidyl peptidase IV. | Ashton, WT., et al. 2004. Bioorg Med Chem Lett. 14: 859-63. PMID: 15012982
- Cinétique de liaison et durée d'action in vivo de nouveaux inhibiteurs de la prolyl-oligopeptidase. | Venäläinen, JI., et al. 2006. Biochem Pharmacol. 71: 683-92. PMID: 16405869
- Activités antidiabétiques, antiglycation et antioxydantes de l'extrait éthanolique de graines de Passiflora edulis et du piceatannol in vitro. | Dos Santos, FAR., et al. 2022. Molecules. 27: PMID: 35807309
- Comparaison in vivo et in vitro du potentiel inhibiteur de la DPP-IV de protéines alimentaires de différentes origines après digestion gastro-intestinale. | Fleury, L., et al. 2022. Int J Mol Sci. 23: PMID: 35955493
Substrat de:
CD26, DPP7, DPRP1, DPRP2, Enzyme, FAP, Fluorogenic, Peptide, POP, et PREP.Informations pour la commande
| Nom du produit | Ref. Catalogue | COND. | Prix HT | QTÉ | Favoris | |
GP-AMC, Fluorogenic Substrate, 5 mg | sc-201157 | 5 mg | CNY1501.00 |
